Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 Re
Re橋本 和幸; Wan, K. W. H. B. B.*; 松岡 弘充
Journal of Nuclear and Radiochemical Sciences, 6(3), p.193 - 196, 2005/12
治療に有効な核的特性を有するラジオアイソトープ(RI)をがんへ集積する性質を有する生理活性物質(モノクローナル抗体等)に標識した化合物は、がんの内用放射線治療への応用が期待されている。メルカプトアセチルトリグリシン(MAG3)は、生理活性物質のRI標識に有用な二官能性配位子の一つである。本研究では、がん治療に有効な核的特性を有するジェネレータ製無担体 ReによるMAG3標識について、直接合成法及び中間体を生成させるtransfer配位子(クエン酸及びグルコン酸)を用いた合成法による標識条件(Reの還元剤である塩化スズ濃度,pH,MAG3濃度,transfer配位子濃度,担体の有無等)の違いを詳細に比較検討した。最適条件下では、いずれの方法によっても90%以上の標識率が得られた。直接法とtransfer配位子法を比較すると、直接法は、反応を窒素気流中で行い、さらに溶媒の除去操作が必要であるが、transfer配位子法では必要がない。したがって、操作上は、transfer配位子法の方が簡便である。また、transfer配位子の違いにより、標識率のpH依存性の違いや室温での反応性の違いなどが観察された。今後は、transfer配位子の違いによる抗体標識及びtransfer配位子を利用した他の有用配位子の標識に関する検討を行う予定である。
ReによるMAG3標識について、直接合成法及び中間体を生成させるtransfer配位子(クエン酸及びグルコン酸)を用いた合成法による標識条件(Reの還元剤である塩化スズ濃度,pH,MAG3濃度,transfer配位子濃度,担体の有無等)の違いを詳細に比較検討した。最適条件下では、いずれの方法によっても90%以上の標識率が得られた。直接法とtransfer配位子法を比較すると、直接法は、反応を窒素気流中で行い、さらに溶媒の除去操作が必要であるが、transfer配位子法では必要がない。したがって、操作上は、transfer配位子法の方が簡便である。また、transfer配位子の違いにより、標識率のpH依存性の違いや室温での反応性の違いなどが観察された。今後は、transfer配位子の違いによる抗体標識及びtransfer配位子を利用した他の有用配位子の標識に関する検討を行う予定である。
上原 知也*; 小池 美穂*; 中田 英夫*; 宮本 重彦*; 本石 章司; 橋本 和幸; 奥 直人*; 中山 守雄*; 荒野 泰*
Nuclear Medicine and Biology, 30(3), p.327 - 334, 2003/04
被引用回数:20 パーセンタイル:50.16(Radiology, Nuclear Medicine & Medical Imaging) Re標識低分子化抗体やペプチドによる癌の治療には、腎臓への放射能集積を示さない一方で、癌組織には長時間に渡る選択的な放射能集積を与える標識体の設計が必要である。そのためには、生体内で安定であり、かつ尿細管で母体タンパク質から遊離された際に、腎細胞へ取り込まれることなく、速やかに尿中へと排泄を受けるRe錯体の選択が重要である。本研究では、Cyclopentadienyltricarbonylrhenium(CpTR)をタンパク質やペプチドの
Re標識低分子化抗体やペプチドによる癌の治療には、腎臓への放射能集積を示さない一方で、癌組織には長時間に渡る選択的な放射能集積を与える標識体の設計が必要である。そのためには、生体内で安定であり、かつ尿細管で母体タンパク質から遊離された際に、腎細胞へ取り込まれることなく、速やかに尿中へと排泄を受けるRe錯体の選択が重要である。本研究では、Cyclopentadienyltricarbonylrhenium(CpTR)をタンパク質やペプチドの Re標識薬剤へ応用する目的で,CpTR-COOH及びそのグリシン(Gly)結合体の生体内での代謝を検討した。その結果、両者はともに血漿中及び緩衝液中で安定であった。一方、マウスに投与した場合、脂溶性の高いCpTR-COOHは胆汁排泄と尿排泄を受けたが、水溶性の高いCpTR-Glyは尿排泄のみを受けた。さらにCpTR-COOHは、複数の水溶性代謝物として排泄されるのに対して、CpTR-Glyは、代謝を受けずにそのまま排泄された。これらの結果から、腎臓刷子縁膜酵素の作用で母体ペプチドから[
Re標識薬剤へ応用する目的で,CpTR-COOH及びそのグリシン(Gly)結合体の生体内での代謝を検討した。その結果、両者はともに血漿中及び緩衝液中で安定であった。一方、マウスに投与した場合、脂溶性の高いCpTR-COOHは胆汁排泄と尿排泄を受けたが、水溶性の高いCpTR-Glyは尿排泄のみを受けた。さらにCpTR-COOHは、複数の水溶性代謝物として排泄されるのに対して、CpTR-Glyは、代謝を受けずにそのまま排泄された。これらの結果から、腎臓刷子縁膜酵素の作用で母体ペプチドから[ Re]CpTR-Glyを遊離する標識試薬は、腎臓での放射能滞留の解消に有用と考えられる。
Re]CpTR-Glyを遊離する標識試薬は、腎臓での放射能滞留の解消に有用と考えられる。
 Re and recovery of tungsten from spent
Re and recovery of tungsten from spent  W/
W/ Re generator
Re generator小林 勝利; 本石 章司; 照沼 久寿男; Rauf, A. A.*; 橋本 和幸
Radiochemistry, 42(6), p.551 - 554, 2000/12
がんの診断・治療用に注目されている Re,
Re, Reの供給のため製造技術を開発した。最初に、
Reの供給のため製造技術を開発した。最初に、 W(p,n)
W(p,n) Re反応による製造法を述べるとともに、主として原子炉による
Re反応による製造法を述べるとともに、主として原子炉による Re,
Re, Reの製造工程(照射、化学分離・精製、放射能測定)、装置及び製品仕様などについて報告する。いずれも安定濃縮同位体である
Reの製造工程(照射、化学分離・精製、放射能測定)、装置及び製品仕様などについて報告する。いずれも安定濃縮同位体である Re及び
Re及び WO
WO を照射し、化学分離・精製後の過レニウム酸水溶液及び
を照射し、化学分離・精製後の過レニウム酸水溶液及び W/
W/ Reジェネレータとして調製した。高価な
Reジェネレータとして調製した。高価な WO
WO の再利用と廃棄物の放射能低減のため、
の再利用と廃棄物の放射能低減のため、 Re及び
Re及び Wをトレーサに用いた模擬ジェネレータを試作し、アルミナカラムからAlを溶離しないでWのみを脱離する条件を検討した。NH
Wをトレーサに用いた模擬ジェネレータを試作し、アルミナカラムからAlを溶離しないでWのみを脱離する条件を検討した。NH OH及びNaOHを溶離剤とし、それぞれ90%または99%以上のWを回収しWO
OH及びNaOHを溶離剤とし、それぞれ90%または99%以上のWを回収しWO として調製後、放射化分析法で純度を確かめた。使用済の
として調製後、放射化分析法で純度を確かめた。使用済の W/
W/ Reジェネレータについて本法を適用し、ターゲットとして再利用できるこが明らかとなった。
Reジェネレータについて本法を適用し、ターゲットとして再利用できるこが明らかとなった。
小川 数馬*; 小野 正博*; 藤岡 泰*; 佐治 英郎*; 向 高弘*; 小西 淳二*; 上原 知也*; 荒野 泰*; 小野間 克行
核医学, 37(5), P. 577, 2000/09
 Reとbisphosphonate(BP)のひとつであるHEDPとの多核錯体である
Reとbisphosphonate(BP)のひとつであるHEDPとの多核錯体である Re-HEDPは、癌性骨転移の疼痛緩和薬剤として期待されているが、生体内での安定性が乏しいことが問題である。そこで生体内で安定な
Re-HEDPは、癌性骨転移の疼痛緩和薬剤として期待されているが、生体内での安定性が乏しいことが問題である。そこで生体内で安定な Re標識骨疼痛緩和剤の開発を目的として、BPの炭素側鎖に
Re標識骨疼痛緩和剤の開発を目的として、BPの炭素側鎖に Reと安定な錯体を形成する部位を結合した化合物を設計した。目的とする化合物は総収率2.7%で合成された。
Reと安定な錯体を形成する部位を結合した化合物を設計した。目的とする化合物は総収率2.7%で合成された。 Re標識は、
Re標識は、 Re標識glucoheptonateとの配位子交換反応により行い、放射化学的純度は95%以上であった。なお、本標識化合物の体内動態については、現在検討をすすめている最中である。
Re標識glucoheptonateとの配位子交換反応により行い、放射化学的純度は95%以上であった。なお、本標識化合物の体内動態については、現在検討をすすめている最中である。
 Re-DMSA and its biodistributions in mice
Re-DMSA and its biodistributions in mice野川 憲夫*; 百瀬 静香*; 宮沢 香*; 巻出 義絋*; 大橋 國雄*; 橋本 和幸; 森川 尚威*
Journal of Radioanalytical and Nuclear Chemistry, 239(2), p.385 - 389, 1999/00
被引用回数:2 パーセンタイル:21.17(Chemistry, Analytical)放射性レニウム( Re,
Re, Re)は
Re)は 線を放出することから、近年、がん治療に有効な標識化合物の開発が行われている。
線を放出することから、近年、がん治療に有効な標識化合物の開発が行われている。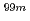 Tc-ジメルカプトコハク酸(
Tc-ジメルカプトコハク酸(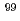 mTc-DMSA)は、腎臓のイメージング試薬として幅広く使用され、さらに、甲状腺がんなどに集積することも知られている。そこで、原研製の
mTc-DMSA)は、腎臓のイメージング試薬として幅広く使用され、さらに、甲状腺がんなどに集積することも知られている。そこで、原研製の Reを用いた
Reを用いた Re-DMSA標識化合物の合成条件を検討し、さらにマウスにおける体内挙動を調べた。反応条件(試薬の量、pH、反応時間等)を変えて
Re-DMSA標識化合物の合成条件を検討し、さらにマウスにおける体内挙動を調べた。反応条件(試薬の量、pH、反応時間等)を変えて Re-DMSAの標識率を調べた。その結果、最適条件下で、95%以上の標識率が得られた。さらに得られた
Re-DMSAの標識率を調べた。その結果、最適条件下で、95%以上の標識率が得られた。さらに得られた Re-DMSAは酢酸緩衝液中及びマウス血清中において安定であることが明らかになった。
Re-DMSAは酢酸緩衝液中及びマウス血清中において安定であることが明らかになった。 Re-DMSAのマウスにおける体内分布に関しては、骨への集積が最も高く、次いで腎臓に集積した。この分布は、
Re-DMSAのマウスにおける体内分布に関しては、骨への集積が最も高く、次いで腎臓に集積した。この分布は、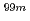 Tc(V)-DMSAの分布に類似していることが明らかになった。
Tc(V)-DMSAの分布に類似していることが明らかになった。
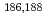 Re for nuclear medicine
Re for nuclear medicine橋本 和幸; 吉原 賢二*
Top. Curr. Chem., 176, p.276 - 291, 1996/00
放射性レニウム( Re、
Re、 Re)は、その優れた核的性質(高エネルギー
Re)は、その優れた核的性質(高エネルギー 線の放出、イメージングに適した
線の放出、イメージングに適した 線の放出など)及びその化学的性質(テクネチウムとの類似性)から、核医学の治療の分野で有望視されている放射性核種である。そこで、本稿では、核医学における
線の放出など)及びその化学的性質(テクネチウムとの類似性)から、核医学の治療の分野で有望視されている放射性核種である。そこで、本稿では、核医学における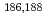 Re標識錯体について、近年の研究成果をまとめた。内容は、以下の通りである。1.放射性レニウム(
Re標識錯体について、近年の研究成果をまとめた。内容は、以下の通りである。1.放射性レニウム( Re、
Re、 Re)の製造
Re)の製造 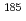 Re(n,
Re(n, )
) Re、
Re、 W(p,n)
W(p,n) Re、
Re、 W(n,
W(n, )(n,
)(n, )
) W
W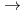
 Re 2.骨ガンの痛みの緩和に有効なレニウム錯体(Re-HEDP,MDP)およびその他の錯体(Re-DTPA,DMSA) 3.二官能性配位子を用いた抗体標識
Re 2.骨ガンの痛みの緩和に有効なレニウム錯体(Re-HEDP,MDP)およびその他の錯体(Re-DTPA,DMSA) 3.二官能性配位子を用いた抗体標識